A ANVISA (Agência Nacional de Vigilância Sanitária) divulgou na última quinta-feira, dia 19/08/2021), o alerta de farmacovigilância relacionado à inclusão de evento adverso grave de hipersensibilidade para o insumo cloridrato de vancomicina do medicamento Vancocina® CP.
Reação adversa de Hipersensibilidade
A Gerência de Farmacovigilância informa a inclusão da reação adversa de hipersensibilidade grave conhecida como DRESS (Drug Reaction with Eosinophilia and Systemic Symptoms ou Reação ao medicamento com eosinofilia e sintomas sistêmicos) na bula do medicamento Vancocina® CP (cloridrato de vancomicina).
Motivo da inclusão da reação adversa
A necessidade de inclusão da reação adversa de hipersensibilidade se baseou em notificação espontânea recebida pela Gerência de Farmacovigilância e verificação de que esta já constava em bases de dados internacionais.
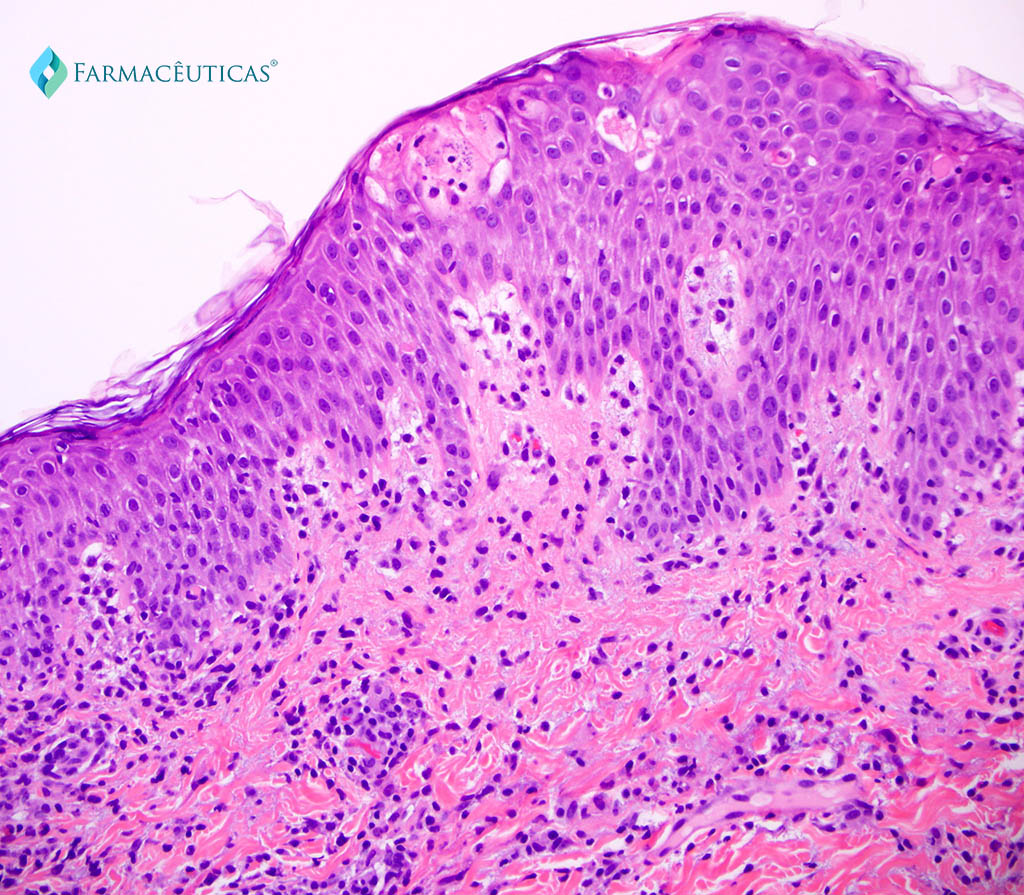
Sobre o DRESS
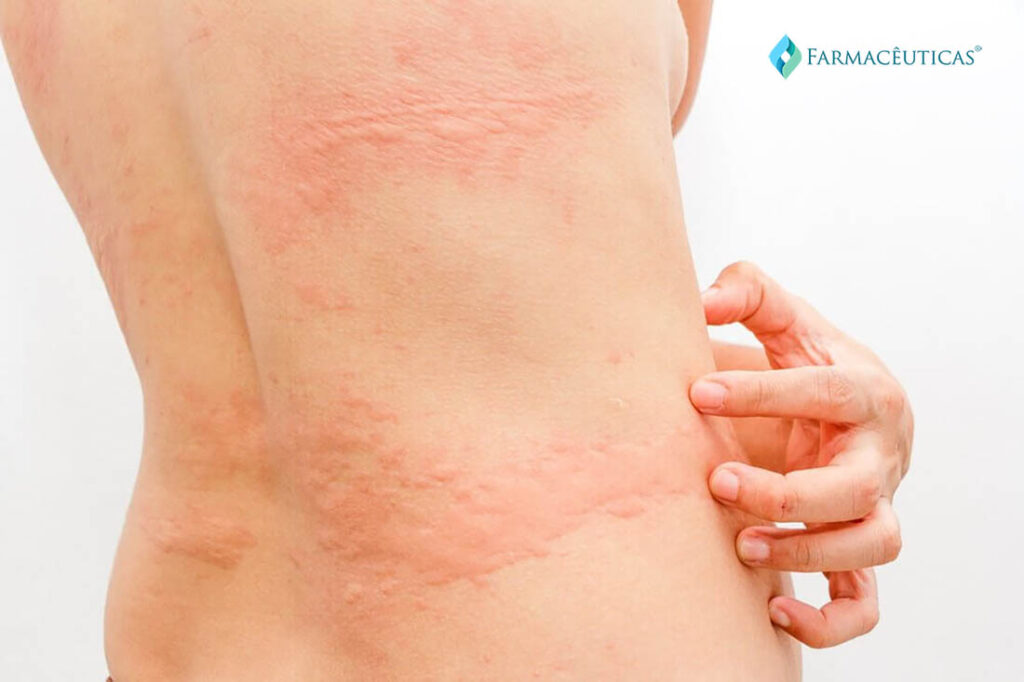
A erupção cutânea por medicamento com eosinofilia e sintomas sistêmicos (síndrome de DRESS), também conhecida como síndrome de hipersensibilidade induzida por medicamento, é uma reação medicamentosa de hipersensibilidade sistêmica grave incomum. Normalmente, se desenvolve 2 a 6 semanas após a exposição ao medicamento causador e se apresenta com erupção cutânea generalizada, edema facial, sintomas sistêmicos (por exemplo, febre, calafrios, hipotensão), linfadenopatia, evidência de envolvimento de órgãos viscerais e, frequentemente, eosinofilia. Os mitos clínicos destacam algumas das suposições comumente aceitas sobre a síndrome de DRESS em um esforço para iluminar as sutilezas do tratamento de pacientes com essa condição. (ISAACS et al, 2018)
Síndrome de hipersensibilidade induzida por medicamento associada à vancomicina
Uma série de casos retrospectivos foi conduzida ao longo de um período de 8 anos em uma única instituição acadêmica. Um total de 29 casos de DIHS / DRESS foram identificados, dos quais 4 foram atribuídos à vancomicina. Foi realizada uma revisão da literatura, na qual identificou 28 casos adicionais de síndromes de hipersensibilidade induzidas por medicamento causada pela vancomicina. A nefrite intersticial aguda associada à vancomicina também foi revisada para detectar casos adicionais não caracterizados de hipersensibilidade sistêmica. A revisão resultou em 11 casos adicionais. (MADIGAN et al, 2019)
Importância dos alertas de farmacovigilância na elaboração e revisão dos relatórios de PDE
O conhecimento de novos eventos adversos de medicamentos, inicialmente não identificados nas fases iniciais dos estudos clínicos e dos estudos pré-clínicos, é adquirido com o passar do tempo, por meio de novos estudos clínicos, principalmente os de fase 4 de pós-comercialização, estudos epidemiológicos e de relatos de casos de eventos adversos graves e não graves publicados. Através da avaliação da frequência e da gravidade do evento adverso, este pode ser classificado como reação adversa (confirmação do evento adverso).
As agências regulatórias (Nacional e Internacionais) publicam alertas de farmacovigilância com a finalidade de divulgação de tais reações adversas, para posterior inclusão da informação na bula do medicamento.
Neste sentido, é importante entender que novos efeitos críticos são descobertos e estes devem ser avaliados por meio dos relatórios de PDE/ADE, justificando, desta forma, a necessidade periódica da revisão das informações contidas nos relatórios de limites de exposição baseados em saúde (HBEL/LEBS) para segurança da saúde dos pacientes e dos colaboradores da empresa.
O conhecimento de novos efeitos críticos, além de levarem à necessidade de revisão dos relatórios toxicológicos (ADE/PDE), demandam a reavaliação do gerenciamento de risco de compartilhamento de área produtiva e implantação de ações para mitigação dos riscos relacionados aos potenciais modos de falhas que podem gerar contaminação cruzada, exposição ocupacional e contaminação do meio ambiente.
Classificação do efeito crítico quanto ao potencial altamente sensibilizante
Classificação quanto ao potencial altamente sensibilizante (reação adversa de hipersensibilidade):
Para a correta classificação quanto ao potencial altamente sensibilizante é necessário avaliar os seguintes dados:
- Gravidade/severidade da sensibilização: A severidade x evidência.
- Frequência: Alta frequência de ocorrências de sensibilização em humanos deve ser considerada.
- Número de casos em humanos: estudos epidemiológicos, relatos de casos publicados e a frequência estabelecida pela farmacovigilância.
- Evidências em modelos animais: Estudos em animais também podem ser úteis para determinar a probabilidade de ocorrência de uma alta sensibilização em humanos. No entanto, para alguns fármacos os efeitos de hipersensibilidade apenas são observados em humanos.
As reações adversas a medicamentos (RAM), principalmente a reação adversa de hipersensibilidade, são causas importantes de morbidade e mortalidade tendo impacto significativo na prática médica diária. (ENSINA et al, 2009)
Referências
ANVISA: Alertas de Farmacovigilância
RESOLUÇÃO DE DIRETORIA COLEGIADA – RDC Nº 406, DE 22 DE JULHO DE 2020. Dispõe sobre as Boas Práticas de Farmacovigilância para Detentores de Registro de Medicamento de uso humano, e dá outras providências.
ISAACS M, CARDONES AR, RAHNAMA-MOGHADAM S. DRESS syndrome: clinical myths and pearls. Cutis. 2018 Nov;102(5):322-326. PMID: 30566546.
MADIGAN LM, FOX LP. Vancomycin-associated drug-induced hypersensitivity syndrome. J Am Acad Dermatol. 2019 Jul;81(1):123-128. doi: 10.1016/j.jaad.2019.02.002. Epub 2019 Feb 6. PMID: 30738120.
ENSINA L. F., FERNANDES F. R., GESU G. D., MALAMAN M. F., CHAVARRIA M. L. , BERND L. A. G. 2009. Reações de hipersensibilidade a medicamentos. Guia prático de alergia e imunologia. Rev. bras. alerg. imunopatol.