QRM X PDE
O compartilhamento de área produtiva sempre foi uma estratégia adotada nas indústrias farmacêuticas para a produção de medicamentos, no qual, o controle de possíveis contaminantes em produtos subsequentes era feito com base nos resultados dos estudos de validação de cada equipamento multipropósito. A questão é que as diretrizes para saber o que era ou não permitido compartilhar, com relação às substâncias ativas, antes estava previsto em normativa. E agora com a publicação da RDC nº 301/2019 e suas respectivas INs o conceito mudou, e o compartilhamento agora deve ser baseado em riscos.
Mas como isso deve ser feito?
A resposta para este questionamento é relativamente simples, mas o o processo de comprovação é complexo, pois é necessário mitigar e gerenciar os riscos relacionados ao compartilhamento em cada etapa da cadeia produtiva dos medicamentos. Além disso, deve haver o estudo de toxicidade por meio do cálculo de PDE de cada molécula/produto.
O que pode ser compartilhado?

Com exceção de moléculas altamente sensibilizantes, como é o caso de antibióticos com anel beta lactâmico (ex: penicilânicos e cefalosporínicos), em tese, as demais substâncias, dentro de uma mesma forma farmacêutica, poderiam ser fabricadas em uma área multipropósito. No entanto, é preciso mitigar os riscos e implementar ações para controlar, e principalmente, prevenir a tendência de ocorrência de desvios. Somente a validação de limpeza não é suficiente.
Na prática, antes de sair criando metas mirabolantes e inconsequentes para produzir novos medicamentos, é preciso planejar cada etapa da cadeia de produção dos medicamentos visando os riscos de ocorrência de contaminação cruzada. Aqui não estamos falando apenas na área produtiva, mas de todos os departamentos relacionados, desde de o recebimento dos insumos ativos, amostragem, análise, pesagem, fabricação até a expedição do produto acabado.
E em termos do que pode e o que não pode, se a empresa comprovar que os riscos são baixos, e que existem mecanismos EFICAZES para detectar os desvios ainda dentro da empresa, e principalmente preveni-los, tudo poderia ser compartilhado, inclusive cosméticos, produtos para saúde, medicamentos veterinários (desde de que tenham uso também em humanos) e alimentos. Nesse sentido, com a RDC 301/2019 e a implantação da atividade de gerenciamento de riscos, a RDC nº 33/2015, que alterava a RDC nº 17/2010 com relação ao compartilhamento de produtos, não se faz mais necessária.
Mas é lógico, se há IFAs comprovadamente tóxicas o risco será altíssimo inviabilizando o compartilhamento, e aqui estamos falando aqui de relatórios de PDE (Permitted Daily Exposure) com resultados inferiores a 10 µg/dia, por exemplo, e com efeitos de carcinogenicidade, mutagenicidade, genotoxicidade, teratogenicidade e toxicidade reprodutiva, além daquelas altamente sensibilizantes, cientificamente comprovados, é claro.
Entendendo o conceito de compartilhamento de área produtiva
O compartilhamento de área produtiva nada mais é do que fabricar diferentes tipos de produtos em um mesmo equipamento e área, sem a necessidade de dedicá-lo (1 IFA por equipamento apenas). No qual, o procedimento de limpeza devidamente validado, até então, era suficiente para garantir a remoção de ativos, agentes de limpeza e microrganismos, até mesmo de endotoxinas, em caso de medicamentos estéreis, a níveis seguros para a paciente, supondo uma possível contaminação cruzada no produto subsequente a ser produzido.
Para entender melhor o compartilhamento é importante pensar nos seguintes pontos destacados abaixo:
- Por quê posso fabricar azitromicina (antibiótico) em uma área de medicamentos MIPs e não posso fabricar amoxicilina (antibiótico)?
- Por quê alguns produtos são manipulados em linhas dedicadas enquanto outros necessitam de prédios/instalações completamente segredadas?
- Qual o risco real de se fabricar cosméticos, alimentos, produtos para saúde e medicamentos veterinários nos mesmos equipamentos de produção de medicamentos?
- A validação de limpeza já não seria suficiente para garantir qualquer risco?
Diante de tais questionamentos, é importante que a empresa entenda que o conceito de compartilhamento mudou, e agora outros pontos que anteriormente não eram considerados devem ser cientificamente comprovados antes de atestar a segurança com relação ao compartilhamento.
Então explicaremos ponto a ponto dos questionamento supracitados:
Explicando o compartilhamento de antibióticos

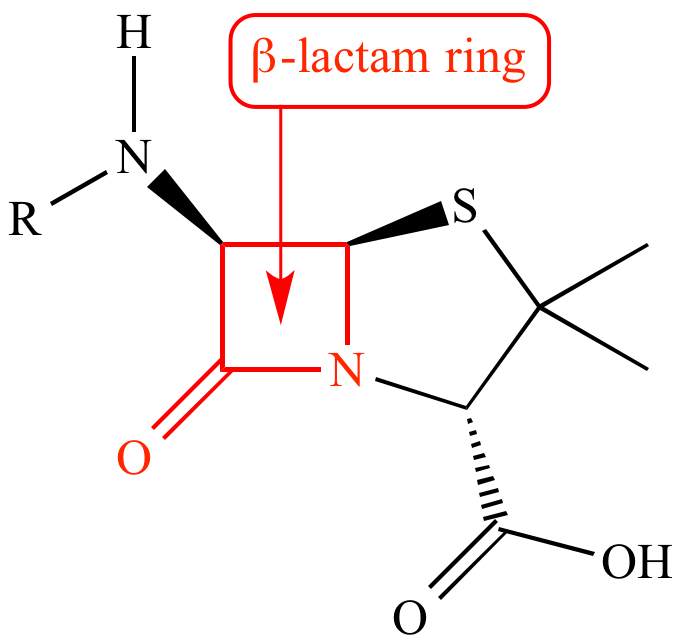
No caso dos antibióticos, aqueles que possuem em sua estrutura química a presença de anel beta-lactâmico, como é o caso dos medicamentos cefalosporínicos e penicilânicos, ainda devem ser segregados dos demais antibióticos, isso porque estes medicamentos são comprovadamente sensibilizantes. Neste sentido, é importante destacar que cerca de 1% a 3% da população possui hipersensibilidade à estas moléculas.
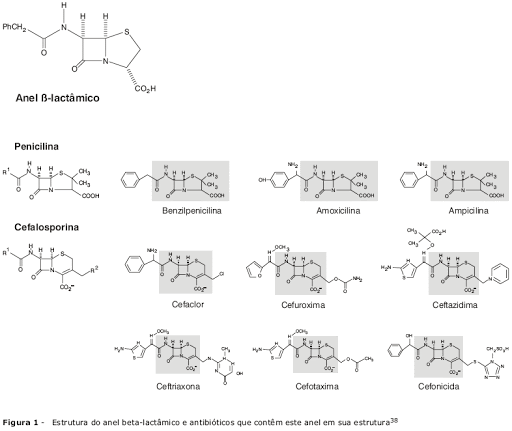
As cefalosporinas são um grupo de antibióticos betalactâmicos derivados do fungo Cephalosporiumacremonium. Tais substâncias se assemelham à estrutura química das penicilinas, apresentando o ácido 7‑aminocefalosporânico (7‑ACA) como núcleo central, constituído por dois anéis, um anel betalactâmico e um anel de di‑hidrotiazina. Todas as cefalosporinas em uso clínico são derivados semissintéticos do 7‑ACA, obtido inicialmente de um antibiótico natural, a cefalosporina C, oriunda deste fungo.
Apesar da comprovação da hipersensibilidade em pacientes, seu uso é justificado por seu amplo espetro de ação, baixa toxicidade, facilidade de administração e perfil farmacocinético favorável.
A alergia à penicilina também pode complicar o tratamento de infecções nas quais uma cefalosporina é o tratamento de escolha do médico. Os dados disponíveis sobre reatividade cruzada e hipersensibilidade simultânea envolvendo esses antibióticos e a penicilina estão incompletos. A literatura atual e passada foi revisada na tentativa de desenvolver abordagens práticas de tratamento e identificar questões clínicas que precisam de mais investigações relacionadas à alergia à penicilina.
Com relação à toxicidade, apesar de ser conhecidamente baixa, se faz necessária a comprovação do valores de PDE e das questões ligadas à sensibilização.
Já os demais antibióticos (aminoglicosídeos, macrolídeos, quinolonas, etc), os relatos de eventos adversos ligados à sensibilização são baixos comparados aos antibióticos betalactâmicos, sendo este motivo pelo qual o risco de compartilhamento é muito baixo se comparado a esta classe em específico.
Áreas multipropósito x áreas dedicadas x áreas segregadas

A determinação do que pode ser ou não compartilhado deve ser feita com base nos resultados do gerenciamento de riscos para compartilhamento de áreas produtivas.
Após a mitigação dos riscos, controles e ações devem ser identificados e detalhadamente analisados para comprovação de um baixo risco permitindo, por exemplo, o compartilhamento. Desta forma, o cenário farmacêutico seria conforme o demonstrado na ilustração abaixo:

A ilustração acima demostra que, de acordo com a toxicidade da IFA, comprovado por meio do relatório de PDE, quanto mais tóxica uma molécula maior deve ser o grau de segurança das utilidades, instalações, paramentação, compartilhamento, e até mesmo a produção em campanha.
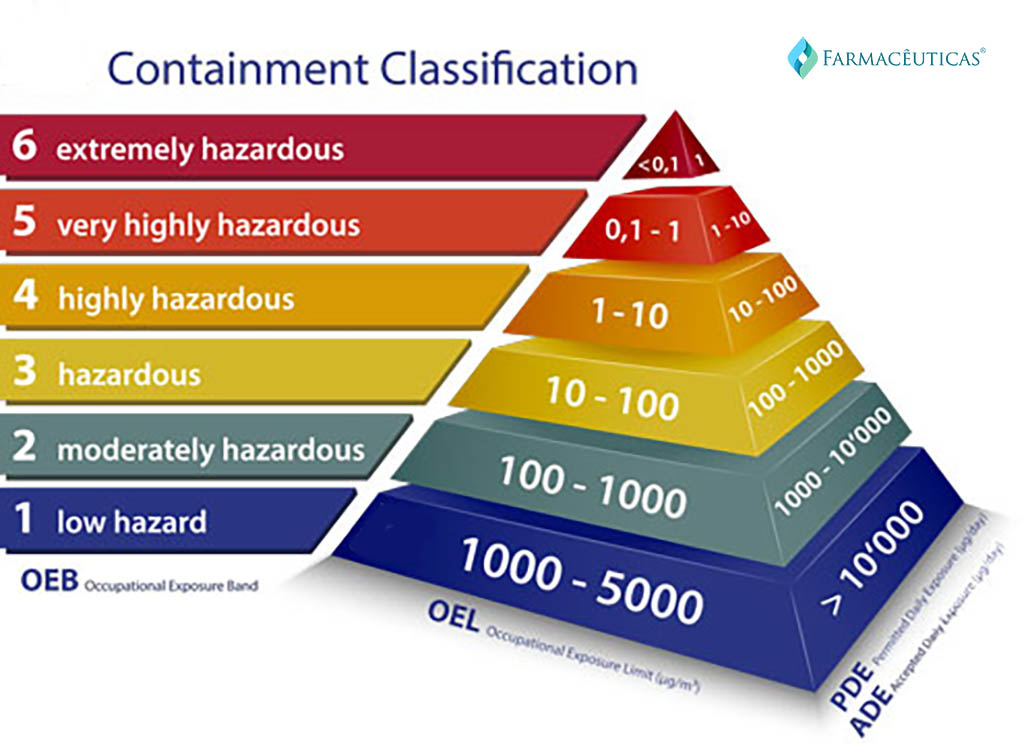
Lembrando que a severidade está relacionada à criticidade dos desvio, enquanto que a ocorrência é medida com histórico dos registros dos desvios de qualidade (não conformidade). O cruzamento das informações, baseados nos controles (detecção) existentes e a serem implantados (ações), é que que determina a classificação do risco inicial e final.
Fabricação de cosméticos, alimentos, produtos para saúde e medicamentos veterinários nos mesmos equipamentos/área de produção de medicamentos

Antes o que era normativo agora deve ser científico, ou seja, a empresa deve mitigar os riscos da cadeia de produção do medicamentos (do recebimento à expedição) e comprovar os controles atuais e a serem implementados de modo que não haja risco de contaminação cruzada em prejuízo à saúde do paciente e do colaborador.
O gerenciamento de riscos de compartilhamento de área é fundamental aqui.
A validação de limpeza é um controle, no qual todos os ativos de cada categoria de produto compartilhado deve ser conjuntamente analisados para identificar o mais crítico de todos, e posteriormente ser submetido ao estudo. Tais controles (relatórios de validação de limpeza) devem ser referenciados tanto na análise de risco quanto no relatório do Gerenciamento de Riscos.
A régua, em termos de nível de qualidade, deve ser a mesma para os medicamentos. Então, não importa se você está produzindo cosméticos, os cuidados sanitários devem seguir o mesmo rigor dos medicamentos, afinal, há o compartilhamento de área produtiva. Caso exista algum cuidado de uma categoria (ex: alimentos – alergênicos), que inicialmente não é exigida para medicamentos, deve ser também adotado para as demais classes de produtos que farão o compartilhamento.
E para aqueles que perguntam sobre o PDE, se há compartilhamento a elaboração desses relatórios é obrigatório, apenas justificado em casos nos quais realmente não há estudos pré-clínicos confiáveis. A justificativa deve ter a comprovação científica atestada pelo toxicologista.
Validação de limpeza e o controle da contaminação cruzada no compartilhamento de área produtiva
Antes somente a validação de limpeza era a garantia da segurança para se evitar a contaminação cruzada no compartilhamento.
Agora, este é apenas mais um dos controles que deve ser referenciado no Gerenciamento de Riscos. A Validação de limpeza sozinha não é mais suficiente.
Aqui se fazem necessários, no minimo, 2 tipos de Gerenciamento de Riscos:
- Gerenciamento de risco de compartilhamento de área produtiva
- Gerenciamento de risco do processo de limpeza (global)
Ah! Não confundir a análise de risco com Gerenciamento de Riscos, por favor!!!
Ainda com relação à VL, não há como atestar segurança se os procedimentos de limpeza não estiverem validados, mas esta validação deve compreender os limites determinados pela dose mínima, critério de 10 ppm e o PDE. Sendo o resultado adotado como critério de aceitação o menor valor obtidos com os cálculos, além de uma análise de risco individual do procedimento de limpeza.
Lembrando que a escolha do pior caso para avaliação da toxicidade também deve ser feita com base no PDE, e não mais pela DL50, uma vez que este representa um índice de morte (Dose letal de 50% de uma população) e não de exposição diária permitida (exposição segura).
Importância do PDE e do Gerenciamento de Riscos para o compartilhamento de área produtiva

Como já coloquei anteriormente o PDE é a base para o compartilhamento, porque avaliaremos a toxicidade da molécula tanto do ponto de vista do paciente quanto em termos de exposição ocupacional (saúde dos colaboradores expostos aos IFAs).
Quanto mais tóxico, maior o risco evidenciado no QRM (Quality Risk Management), e por isso os mecanismos de controles serão maiores.
Resumo dos itens obrigatoriamente avaliados de acordo com a toxicidade:
Soluções físicas e técnicas
- Sistemas fechados
- Single use
- Amostragem fechada
- Antecâmaras
- Sistemas de exaustão e HVAC dedicados e filtro 100%
- Classificação de áreas
- Pressão positiva ou negativa
- Segregação de áreas ou linhas
- Produção em campanha x risco operador
- Materiais em contato com produtos
- Gerenciamento dos resíduos e risco ambiental
Impacto na saúde a ser considerado
- Avaliação da ocorrência e detecção de desvios – Tendência de ocorrência (estatística)
- Procedimentos/ instalação / logística
- Paramentação – Projetar níveis adequados de proteção
- Estudos de qualificação e validação (processo e limpeza – PDE)
- Otimização do fluxo de material
- Recipientes padronizados e fechados – com estudo de HT
- Identificação dos pontos críticos do processo x potencial de contaminação.
Tudo isso devidamente mapeado no Gerenciamento de Riscos considerando-se toda a cadeia produtiva dos medicamentos.
Ajuda para elaboração de relatórios e PDE e de Gerenciamento de Riscos

Espero que o post tenha lhe ajudado, mas sei que dúvidas podem surgir.
Sendo assim, se precisar de ajuda para a elaboração dos projetos de Gerenciamento de Riscos de sua empresa, e até mesmo para a elaboração dos relatórios de PDE, entre em contato conosco:
contato@farmaceuticas.com.br

Referências bibliográficas
- US National Library of MedicineNational Institutes of Health – https://www.ncbi.nlm.nih.gov/
- Jornal de pediatria – Alergia a beta-lactâmicos na clínica pediátrica: uma abordagem prática
- OSHA
- NIOSH
- WHO
- PIC/s





