Serialização e rastreabilidade
A RDC nº 54 de 2013 que determina as novas diretrizes e regras de identificação de um medicamento (IUM), através do conceito de serializiação e rastreabilidade, apesar de amplamente divulgada ainda é de difícil entendimento.
Isso porque além da nova Resolução ter muitos GAPs, ou seja, muitos pontos que ainda não foram totalmente definidos por parte da ANVISA, a própria sistemática para identificação ainda não ficou clara.
Apesar das diversas soluções tecnológicas apresentadas no mercado, a grande verdade é que a maioria das empresas não sabem por onde começar.
Outro fato é a dificuldade de compreensão do verdadeiro conceito de serialização e rastreabilidade.
Diante de tanta polêmica, e até mesmo confusão em termos de entendimento da Norma, é que se faz necessária uma explicação de todo o conceito, metodologia, aplicação, além mostrar as soluções tecnológicas mais completas.
Entretanto, as explicações contidas neste texto servem principalmente para os fabricantes de medicamentos, uma vez que a ANVISA ainda não definiu a sistemática para controle e armazenamento dos dados da parte da cadeia do medicamento que vai desde do operador logístico até as drogarias.
Enfim, as dúvidas são muitas, mas com as informações contidas neste texto o entendimento do processo ficará um pouco mais claro:
SERIALIZAÇÃO E RASTREABILIDADE – RDC nº54 de 2013
Etapas que compõem o processo de Serialização e Rastreabilidade
1. Aquisição de Servidor de Rastreabilidade e Softwares
Antes de iniciar a compra de equipamentos, a empresa tem que reestruturar o servidor e adquirir plataformas e softwares específicos para rastreabilidade.
Sendo assim, é necessário investimento na área de TI (Tecnologia da Informação) para:
- Aquisição de solução para banco de dados;
- Aquisição de Servidor de Rastreabilidade;
- Aquisição de software ou plataforma de rastreabilidade para o funcionamento dos equipamentos de serialização;
- Aquisição de sistema de visão, inspeção de dados e rejeição de produtos;
- Realizar a integração entre software de gestão das linhas com o ERP vigente.
NOTA: ERP (Enterprise Resource Planning) é um sistema de informação que integra todos os dados dos materiais, processos produtivos, análises, status e estocagem de produtos fabricados por uma indústria em um único sistema.
1.1 Funções do servidor, integração com o ERP e software de rastreabilidade
Servidor de rastreabilidade: responsável por gerar o número serial único do medicamento que será codificado na unidade do medicamento (ex: cartucho).
Também é no servidor que os dados gerados durante os processo de serialização e de rastreabilidade na linha de embalagem serão disponibilizados para posterior envio ao banco de dados.
Integração com o ERP: Para que os dados de lote sejam informados ao sistema de Serialização e Rastreabilidade, é necessária que haja interface do mesmo com o software de ERP (ex.: SAP®).
Software de Rastreabilidade: Plataforma / software de rastreabilidade
- Recebe os números de série gerados pelo servidor de rastreabilidade;
- Recebe os dados produtivos do sistema ERP;
- Compila as informações do servidor e do ERP e cria o código em 2D DATAMATRIX (bidimensional);
- Fornece os dados no formato padronizado pela RDC nº 54/2013 para impressão do lote, número de registro da ANVISA, datas de fabricação e validade;
- Envia os dados obtidos na linha para o servidor de rastreabilidade;
- Gera etiqueta para identificação das caixas de embarque e dos paletes (agregação)
Software para sistema de inspeção de dados:
- Realiza a inspeção dos dados codificados;
- Faz a rejeição unidade com falhas;
[quote_center]Fique de olho: Dependendo da marca de Equipamento de serialização o software de gestão de linha não se comunica diretamente com servidor de rastreabilidade. Neste caso é necessário a aquisição de um servidor extra para fazer a ponte entre o software de rastreabilidade e o servidor.[/quote_center]
Desvantagens do uso de servidor extra:
- Mais custos para adequadação do servidor de rastreabilidade
- Cria dependência do processo
- Este tipo de servidor gera número de série em duplicidade – redundante
- Limitação de licença. No caso de aquisição de novos equipamentos, deve haver aquisição de novas licenças.
No caso do software LineMaster® fabricado pela Optel Vision® a comunicação dos equipamentos com o servidor é direta, não precisa de um servidor extra.
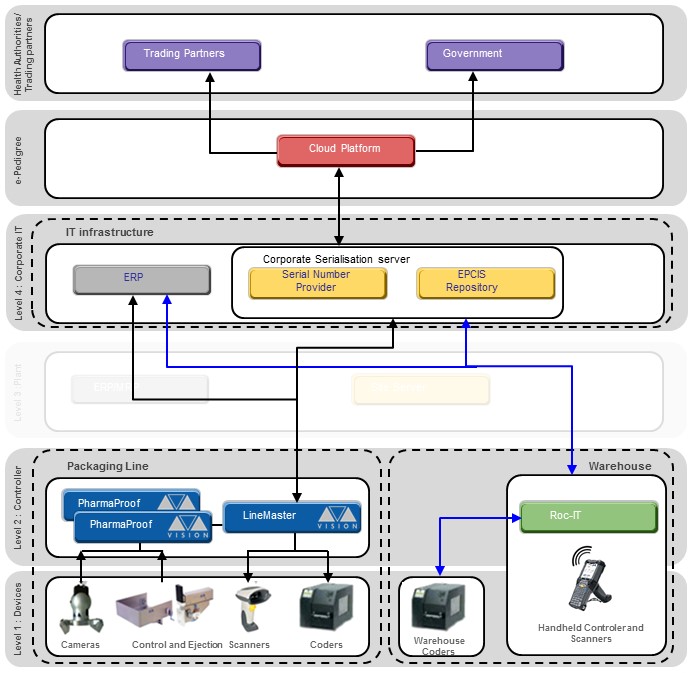
Ilustração da Arquitetura do TI para o sistema de serialização e rastreabilidade. Arquitetura Optel Vision®, sem level 3 (Nível 3 – servidor extra).
2. Como gerar o Identificador Único de Medicamentos (IUM) para adequação da RDC nº 54/2013 – IUM
O Identificador Único de Medicamentos (IUM) é formado pelo cruzamento do Número de Registro do Medicamento fornecido pela ANVISA com o número de série único gerado pelo processo de serealização na etapa de codificação da unidade do medicamento.
RDC nº 54/2013 – do Sistema de Identificação Exclusivo (IUM)
Art. 6º O IUM deve ser formado pelos dados abaixo dispostos, obrigatoriamente, na seguinte ordem:
I – Número do registro do medicamento junto à Anvisa,contendo 13 (treze) dígitos
II – Número serial
III – Data de validade, no formato MM/AA e
IV – Número do lote.
O Registro do Medicamento será sempre o mesmo de acordo com o registro do produto na ANVISA.
O Número Serial deverá ser diferente para cada unidade produzida do medicamento;
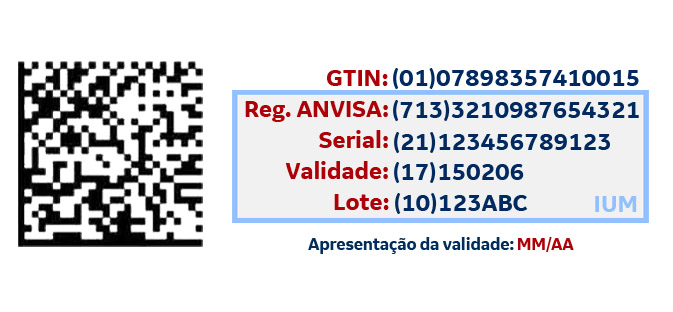
Exemplo de IUM
Exemplo de como é formado o Identificador Único de Medicamentos (IUM)
OBS: GTIN é uma padrão de identificação do GS1 (Instituição que padroniza códigos de barra, datamatrix e outros tipos de códigos). Este número não precisa constar no cartucho.
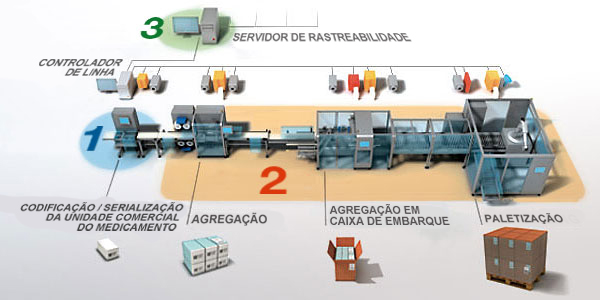
3. Etapa produtiva
A sistemática de serialização e rastreabilidade tem início na etapa de embalagem do medicamento.
É nesta etapa do processo produtivo do medicamento onde todos os dados referentes à produção do lote (separação da matéria-prima, pesagem, dados da produção do semi-acabado, reconcialiação, liberação, entre outras informações), serão inseridos no sistema de codificação chamado DATAMATRIX.
Além do código, é necessária a criação de um número serial único para cada unidade de medicamento.
Também é necessária a inclusão do número do Registro do medicamento na ANVISA, inclusão do número de lote, e datas de validade e fabricação.
Exemplo de código bidimensional (2D) do tipo DATAMATRIX
4. Serialização e Rastreabilidade
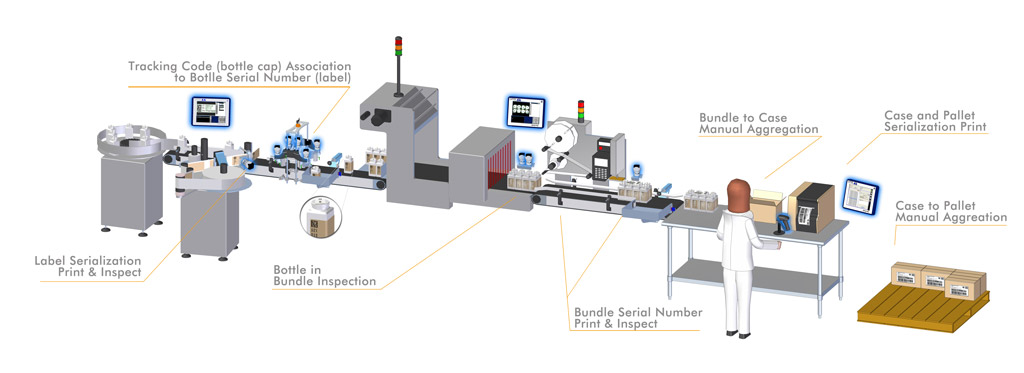
O processo todo de serialização e rastreabilidade é composto das seguintes etapas:
1º Serialização
2º Agregação
4.1 Serialização
Durante a fase de codificação, onde normalmente são inseridos os dados referentes ao lote, datas de fabricação e validades (rotulagem, blistagem para produtos de dose unitária) a partir desta Norma, deverão conter, além destas informações básicas, todos as informações referentes às fases anteriores do processo. Mas isso só é possível a partir deste sistema de codificação, chamado DATAMATRIX (2D).
Além do código gerado em 2D (bidimensional), o sistema deve ser capaz de gerar um número serial único para cada unidade de medicamento produzida.
A etapa de serialização consistente basicamente em duas fases:
1º Serialização – criação da codificação/ número de série (IUM)
2º Inspeção do dados impressos e rejeição, em caso de falhas.
4.1.1 Serialização
É a atribuição e aplicação de um identificador único às embalagens unitárias de medicamentos (Número Serial), ou seja, é a impressão do código (2D) e dos dados produtivos do lote.
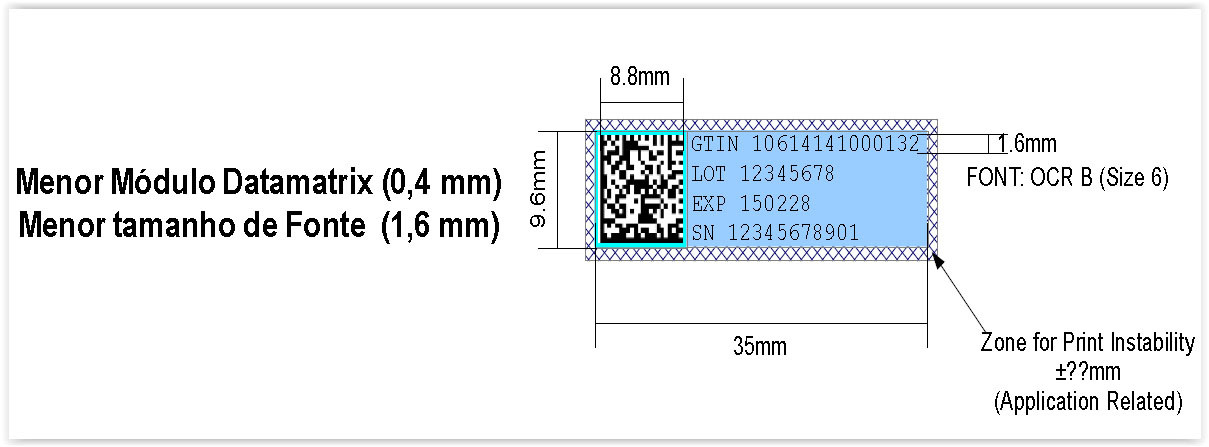
A impressão dos dados deve ser feita no cartucho ou na menor dose comercializada para o consumidor final/paciente (ex. blister com dois comprimidos vendido em balcão de drogaria – dose unitária). O equipamento deve ter capacidade para imprimir os dados tanto do DATAMATRIX, número do registro do produto na ANVISA, numero serial, além do lote e datas de validade e fabricação, com alto padrão de qualidade.
Exemplo do menor tamanho de fonte e DATAMATRIX possíveis para a codificação/serialização da menor dose comercial do medicamento (ex. Amostras grátis, blíster com 2 unidades, etc) – Opção oferecida pela OptelVision®
[quote_center]Nota: certifique-se de que o equipamento a ser adquirido para a impressão da codificação, segundo a RDC nº 54/2013, possui qualidade de impressão necessária segundo o tamanho da menor unidade de medicamento comercializada de sua empresa.[/quote_center]
4.1.2 Inspeção dos dados impressos
O equipamento de serialização deve conter sistemas de inspeção visual e rejeito eficientes para que todos os dados impressos estejam dentro dos critérios de aceitação estabelecidos na Norma RDC nº 54 de 2013. São eles:
- Ajuste do tamanho da impressão
- Qualidade da impressão
- Leitura dos dados para para comparação entre os dados fornecidos pelo sistema de ERP com o impresso
- Rejeição em caso de falhas na impressão ou divergência nos dados impressos
4.2 Agregação
4.2.1 Agregação da unidade do medicamento na caixa de embarque
Após a codificação dos dados de serialização no cartucho, as unidades de medicamento devem ser agregadas (colocadas) em uma mesma caixa de embarque de modo a pertencerem uma mesma família ou grupo.
Cada nível/fileira de cartucho agregados devem ser fotografados, seus dados inspecionados e armazenados até a composição final da caixa de embarque.
Após completar a caixa de embarque com a totalidade de unidades de medicamento, o sistema deve emitir uma etiqueta no qual ficará armazenado os dados de todas unidades que compõem a caixa, além de gerar um novo código (pai). Esta etiqueta “pai” deve ser colada na caixa de embarque para identificar os “filhos”.
Exemplo de etiqueta de agregação que deve ser colada na caixa de embarque (pai) contendo os cartuchos/medicamentos (filhos)
Resumindo:
- A agregação é uma etapa que consiste na associação de unidades com identificações únicas e exclusivas (filhas), para formar uma nova unidade (pai);
- Essa nova unidade, formada por unidades menores, deverá receber identificação única (numérica) e exclusiva para rastreamento;
Todos os dados impressos gerados durante o processo de serialização devem ser armazenados e enviados de volta ao servidor de rastreabilidade.
4.2.2 Agregação em Palete – Paletização
A RDC nº 54 de 2013 não é mandatória com relação ao requisito de agregação das caixas de embarque no palete, mas como o controle e rastreabilidade dos dados de todas as etapas produtivas devem ser armazenados e enviados ao banco de dados do servidor de rastreabilidade do fabricante, com posterior envio das informações para o banco de dados da ANVISA (ainda sem definição de como vai funcionar), esta etapa se torna fundamental.
Sendo assim, o ideal é que todas as caixas de embarque contendo o número de identificação (pai) sejam inspecionadas e os dados armazenados para facilitar as rastreabilidade dentro da área de armazenamento, com posterior envio do palete para o operador logístico/cadeia logística.
Para tanto, após a inpeção e coletas de dados das caixas de embarque, nova etiqueta deve ser impressa contendo todas as informações das unidades de pais e filhos, e esta deve ser colada em local visível após “stretching” ou “strecht wrap”(colocação de strectch film) para proteção das caixas de embarque.
Para melhor compreensão de todo o processo de serialização, inspeção e agregação, assista ao vídeo a seguir:
Resumo das aquisições iniciais do fabricante
1º Aquisição e instalação de servidor de rastreabilidade pela empresa fabricante para gerar número serial único e armazenar dados da de serialização e rastreabilidade (reconciliação).
2º Aquisição do software de serialização rastreabilidade (ex: LineMaster® da Optel Vision®) que faça a interface entre:
- Servidor de rastreabilidade
- Sistema de ERP
- Equipamentos (software) de serialização e inspeção de dados para rastreabilidade
3º Aquisições de equipamentos de serialização e inspeção de dados rastreabilidade e impressão de acordo com o tipo de linha de embalagem, depósito e áreas físicas disponíveis
- Linha de Embalagem Automática
- Linha de Embalagem Semi-automática
- Linha de Embalagem Manual
- Áreas de separação de pedido para envio de produto para o operador logístico
- Área de devolução – conferência de materiais devolvidos
- Estações de Retrabalho – equipamentos portáteis
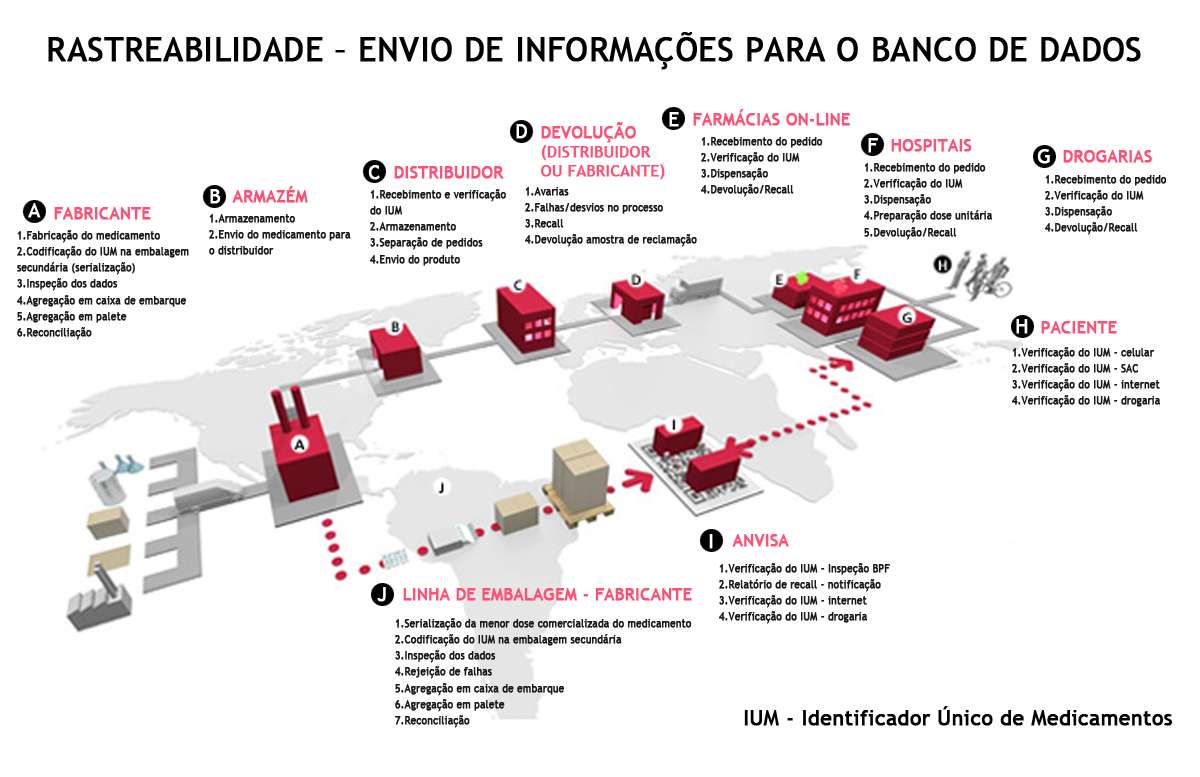
Esquema da cadeia de medicamentos
Vantagens do novo sistema de serialização e rastreabilidade
- Cada medicamento terá identificação única;
- Cada etapa estará registrada e será passível de verificação;
- Acompanhamento desde a etapa de embalagem até o consumidor final;
- Produtos falsificados ou roubados poderão ser identificados – alerta de duplicidade em caso de produto clonado;
Sistema atual de rastreabilidade por Código de Barras
O sistema atual de código de barras é eficaz mas limitado em termos de armazenamento de dados de rastreabilidade.
O sistema atual é composto por:
- Código de Barras;
- Data de Validade;
- Lote;
Vantagens (permite):
- Permitem Recall de todo lote;
- Gerenciamento de inventário;
Desvantagens (NÃO Permite):
- Identificação de produtos falsificados;
- Identificação de produtos roubados;
- Rastreabilidade do produto;
Dúvidas, Respostas e GAPs da RDC nº 54/2013
Apesar do pouco tempo ainda restante para a adequação à RDC nº 54 de 2013 pelas empresas fabricantes, e de toda a cadeia do medicamento, ainda existem lacunas (GAPs) a serem definidos, principalmente pela ANVISA.
Principais dúvidas e algumas respostas
-
Quem desenvolverá a nuvem (banco de dados central)?
R: De acordo com o último evento GS1, o banco de dados será fornecido por empresas privadas, que deverão ser homologadas.
-
Quem será responsável pela nuvem de armazenamento de dados e informações referentes à cadeia do medicamento? ANVISA?
R: Responsável pelo banco de dados é o detentor do registro.
-
De que maneira as distribuidoras e drogarias enviarão as informações referentes aos medicamentos para a nuvem?
R: Os dados serão enviados via arquivos tipo xml, conforme instrução normativa IN 06/2014.
Os eventos ou processo que ocorrem no decorrer da cadeia de medicamentos devem ser transmitidos em tempo real ao detentor do registro do produto e ao elo precedente da cadeia no momento em que forem registrados no banco de dados.
A transmissão da declaração de eventos deverá assegurar ao detentor do registro o acesso a qualquer momento dos dados posteriormente declarados, inclusive nos casos eventuais problemas de conectividade, mesmo que temporários, posteriormente ocorridos entre o detentor do registro e o elo.
-
Quais serão os dados referentes à produção de medicamentos enviados para a nuvem?
R: Dados estão na instrução normativa IN 06/2014.
-
Quais os dados serão enviados da drogaria para a nuvem?
R: Estão na instrução normativa IN 06/2014.
-
Quanto tempo os dados devem ficar armazenados?
R: Os registros dos dados devem permanecer armazenados e à disposição das autoridades sanitárias pelo período de um ano após a expiração do prazo de validade do medicamento, conforme disposto no artigo 15 da RDC nº 54 de 2013 e no § 7º do artigo 205 da RDC 17/2010.
Durante este período deve ser garantido o rastreamento dos dados e eventos comunicados pelos elos posteriores.
Em casos de indisponibilidade temporária ou permanente de dados, inclusive por caso fortuito ou força maior, deverão ser prontamente notificadas à Anvisa.
-
Quais são os equipamentos e softwares nos quais as distribuidoras e drogarias terão que adquirir?
R:
Distribuidoras: Servidor Repositório e equipamentos e sistemas capazes de realizar o recebimento, gerenciamento da unidade, retrabalho, envio, recolhimento e destruição. Leitores portáteis. Ex: Soluções da ROC IT® http://www.rocitsolutions.com/
Drogarias: Servidor Repositório e leitores manuais;
Farmácias on-line: Servidor Repositório e leitores manuais;
-
As drogarias e distribuidoras terão que adquirir um servidor de rastreabilidade? Qual seria este servidor?
R: A principio ficou definido que as distribuidoras, farmácias on-line e drogarias terão de possuir um Servidor Repositório.
GAPS
-
As distribuidoras e drogarias terão acesso às informações da fase produtiva do medicamento?
R: É provável que não. Até onde se sabe as empresas da cadeia receberão os números de série e enviarão de volta o relatório de reconciliação para o banco de dados.
-
Até que ponto a Anvisa terá acesso as informações na íntegra decorrente do processo produtivo armazenados na nuvem?
R: Ainda não foi esclarecido.
-
Em caso de Recall (Recolhimento de mercado), como será feito o envio das informações do medicamento recolhido da drogaria para o operador logístico e deste para a empresa fabricante (logística reversa)?
R: Ainda não foi esclarecido.
-
O custo do investimento para adequação à Norma terá impacto no custo do medicamento?
R: Muito provavelmente sim. Como o preço dos medicamentos é regulado pelo Governo, não há como ter uma afirmação concreta sobre o possível aumento.
-
O consumidor/paciente conseguirão obter informações dos dados da cadeia ou do medicamento através de aplicativo de smartphones como acontecem em outros países?
R: Ainda não foi esclarecido.
-
Como funcionará em hospitais? Englobará também o fracionamento de medicamentos?
R: Pelo conceito sim, mas as últimas informações que surgiram sobre o assunto é que somente será registrada a entrada do medicamentos no hospital. Nas regras atuais o número serial precisa ser rastreado até a entrada no hospital ou farmácia (ponto de dispensação) e somente no nível da embalagem secundária. A partir do momento que o estabelecimento fraciona o medicamento a rastreabilidade é perdida.
Soluções Tecnológicas para adequação à Norma RDC nº 54 de 2013
A Optel Vision® possui soluções tecnológicas de serialização, inspeção de dados, rastreabilidade e impressão para as seguintes áreas:
- Software para inspeção de dados em linha de Embalagem – Pharma Proof®
- Software para serialização em níveis e controle de agregação – Track Safe™
- Software de rastreabilidade – LineMaster®
- Equipamento para linha de embalagem automática – Cartuchos
- Equipamento para linha de embalagem automática – Frascos
- Equipamento para linha semi-automática e manual de embalagem
Flying Carton Tracker® – serialização e inspeção de dados
Pack Station® – agregação das unidades de medicamento para caixas de embarque
Carton Tracker™
Pack Station™
Agregação em paletes
Leitores portáteis – inspeção de dados e armazenamento
Leitor fixo
- Paletização
Agregação em paletes
- Estações de retrabalho – Devolução
Pack Station™
Leitores portáteis – inspeção de dados e armazenamento
Leitor fixo
- Drogarias, Farmácias on-line e Hospitais
Leitores portáteis – inspeção de dados e armazenamento
Leitor fixo
Vantagens da Optel Vision®
A Optel Vision® possui o mais completo conjunto de soluções tecnológicas para a adequação à Norma RDC nº 54/13 referente à serialização e rastreabilidade.
São mais de 60 tipos diferentes de ferramentas de inspeção de dados que podem ser adaptados aos processos de embalagem.
Além de melhor solução tecnológica para adequação de linhas, os equipamentos da OptelVision® ainda oferecem as seguintes vantagens:
- Geração antecipada de Números Seriais;
- Números Seriais armazenados nas linhas, com “pool” de mais de uma semana;
- Continuidade do Processo em caso de falhas no servidor;
- Redução do risco de paradas não programadas;
- Emissão de Relatório de Reconciliação de lote;
- Emissão de Relatório de Performance Padronizados (motivos de hora parada e produtividade);
- Permite padronização dos relatórios para atendimentos às necessidades do sistema de gestão de qualidade do fabricante;
- Emissão de Relatória Análise Estatística;
- Não precisa de aquisição de servidor extra;
- Os equipamentos da Optel Vision® podem ser adequados à plataforma (software) de serialização já existente;
- Não necessitam de licença de uso;
- Adequação ao CFR 21, parte 11;
- Serialização em níveis;
- Controle da agregação;
- Retrabalhos de forma rápida e segura;
- Controle de amostragens;
- Suporte técnico:
Engenharia e suporte técnico local
Documentação de Qualificação e Validação em Português
Equipe especializada em Qualificação e Validação de Sistemas Computadorizados
Suporte Telefônico e Remoto sem custos
Agora que compreendeu melhor a sistemática de serialização e rastreabilidade, entre em contato com um dos representantes dos equipamentos da Optel Vision® e veja as propostas para soluções tecnológicas que melhor se adequam às necessidades do seu processo:
Referências
RDC nº 54 de 2013 -ANVISA
IN 06/2014 – ANVISA























Gostei muito, o controle desta RDC 54/2013 fará com que inibição de falsificação seja rigorosa. Medicamento é produto sério…
Oi, Anselmo!
A intenção da RDC 54/2013 é realmente inibir, ou pelo menos diminuir/dificultar, a falsificação de medicamentos. Além de aumentar a segurança e a qualidade dos produtos farmacêuticos produzidos. Agora, o mais importante é o banco de dados a respeito da produção e a rastreabilidade de cada unidade. Será um grande avanço para a área da saúde brasileira.
Agora devemos ficar atentos porque em 2015 deverão ser iniciados os primeiros testes para verificar se a nova sistemática realmente funciona. Mas será que todas as indústrias, hospitais, drogarias e distribuidoras estão preparadas?
Infelizmente, a maioria nem se quer começou a buscar as informações a respeito do assunto.
É o terrível hábito, se assim podemos chamar, do brasileiro de deixar tudo para a última hora…
De qualquer maneira, estarei aqui para ajudar e divulgar informações valiosas a respeito do assunto.
Abraços.
[…] Aliás, algumas dúvidas, perguntas e respostas já haviam sido expostas no artigo Serialização e rastreabilidade – Estratégias para a implementação do sistema e adequação à…. […]
[…] das soluções é o CaseTracker® , da americana Optel Vision, que identifica quais itens são embalados em conjunto. Ele possui tecnologia de leitura TrackSafe […]
[…] Vision, empresa canadense com 25 anos de história, líder em Serialização e Rastreabilidade nos EUA, traz sua mais recente inovação para FCE Pharma: o Flying CartonTracker ™. Trata-se de […]
[…] as operações devem ser registradas para que seja garantida a rastreabilidade dos […]
[…] Serialização e rastreabilidade – Estratégias para a implementação do sistema e adequação à… […]
[…] Leia mais sobre a RDC nº 54 e as alterações necessárias em http://www.farmaceuticas.com.br/rdc-542013-anvisa-sem-misterios/ http://www.farmaceuticas.com.br/estrategias-para-implementacao-sistema-de-serializacao-e-rastreabili… […]