O cálculo desenvolvido por Destin LeBlanc para determinar o limite de aceitação de resíduos para uma validação de limpeza ficou mundialmente conhecido e é amplamente utilizado pelas indústrias farmacêuticas.
Para quem nunca teve acesso ao cálculo na íntegra, aqui vai um resumo dos principais pontos deste estudo:
Determinando o limite no produto subsequente (LSP – Limit in subsequent product)

O ponto inicial para determinação do limite de aceitação é o quanto de resíduo de um produto poderá passar para o lote subsequente, após a limpeza de um determinado equipamento, sem que haja risco de contaminação a nível prejudicial para a saúde de um paciente.
Para o cálculo:
- Qualquer princípio ativo pode estar presente no produto subsequente num nível máximo de 10 ppm.
- Qualquer princípio ativo pode ter no máximo de 1/1000 ppm da dose mínima diária dentro da dose máxima diária do produto subsequente.
Complicado?
Vamos ao desenho:
Rota de produção do equipamento em estudo (Produtos) 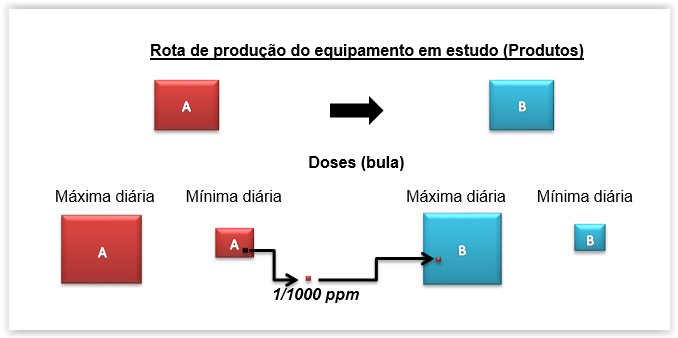
Onde: Produto A (mais crítico) – ativo de escolha da validação (análise de risco – pior caso)
Produto B – produto subsequente
L1ou LSP = Limite no produto subsequente (mcg/mL; mcg/g)
Fórmula:

Dose mínima do ativo pior caso – mcg/dia = Concentração do ativo A por dose unitária (mcg/g ou mcg/mL) x Quantidade por dose (g/dose ou mL/dose) x número mínimo de doses ao dia (dose/dia).
NOTA: caso deixe a mínima dose expressa em mg, não se esqueça de multiplicar por 1000 para transformar em mcg (microgramas).
Dose máxima do PRODUTO (e não do ativo) subsequente – g/dia; mL/dia = Quantidade por dose (g/dose ou mL/dose) x número máximo de doses ao dia (dose/dia).
Fator de Segurança segundo a via de administração mais crítica (do pior caso ou do pior subsequente).
FATOR DE SEGURANÇA
1/100 (0,01) da menor dose diária – Produtos tópicos (dérmicos).
1/1.000 (0,001) da menor dose diária – Produtos orais, inalatórios, vaginais e retais.
1/10.000 (0,0001) da menor dose diária – Produtos injetáveis, oftálmicos e imunossupressores.
Escolha do Limite Residual da Substância Ativa do Produto manipulado no Produto manipulado subsequente (LPPm):

Cálculo para determinação do limite Residual da Substância Ativa do Produto por área superficial (LAS ou L2)

Onde 1000 é o fator de conversão de Kg para g
LAS ou L2= Limite da área de superfície amostrada
Limite na Análise da Amostra (LAA ou Cálculo para determinação do Limite Residual da Substância Ativa do Produto por Área Amostrada (LAA ou L3)
Para o cálculo de LeBlanc na validação de limpeza será considerada a técnica direta de amostragem por swab. O limite será determinado através do cálculo abaixo que deverá ser aplicado para todos os possíveis produtos subsequentes, INCLUINDO O PIOR CASO:

No entanto, para a técnica de amostragem por rinsagem o cálculo é um pouco diferente:

Importante destacar que o método do pior caso deve ser sensível o suficiente para (LD e LQ do método menor que o critério de aceitação do limite de residual calculado) determinar de forma precisa o resultados das amostras de validação de limpeza.
Lembrando que o cálculo deve ser executado para o pior caso combinando todos os possíveis produtos subsequentes (produto B).
Entretanto, é possível facilitar o cálculo utilizando a estratégia de escolha do pior subsequente matemático:

Dessa forma, a escolha do pior subsequente matemático é determinada através da menor razão entre o tamanho lote e a maior dose terapêutica de cada produto/princípio ativo.
Talvez todos esses cálculos pareçam complicados em um primeiro momento, mas se tiver qualquer dúvida fique à vontade para nos contatar: contato@farmaceuticas.com.br
Abs,
Fernanda de Oliveira Bidoia






[…] uma amostragem, sendo esta por swab (método direto) ou por rinsagem (método indireto), mediante cálculo de comparação do limite aceitável e resultados das análises das amostras do Controle de […]