Diante da polêmica envolvendo a Fosfoetanolamina, entre outras situações como os nutracêuticos, a Anvisa publicou na última quinta-feira uma passo a passo para trazer maiores esclarecimentos sobre os procedimentos necessários para o registro de medicamentos na Agência em todo território nacional. As informações e diretrizes são baseadas na Lei nº. 5.991/1973, que determina que [quote_center]medicamento é todo produto farmacêutico, tecnicamente obtido ou elaborado, com finalidade profilática, curativa, paliativa ou para fins de diagnóstico.[/quote_center]
Assim, qualquer produto, independentemente da natureza (vegetal, animal, mineral ou sintética) que possuir alegações terapêuticas, deve ser considerado medicamento necessitando, obrigatoriamente, de registro para ser fabricado e comercializado.
É importante esclarecer que, antes de começar a testar novos medicamentos em seres humanos, devem ser realizados os estudo não clínicos, os quais são realizados em laboratórios e em animais de experimentação.
Os estudos são inicialmente realizados em animais e em laboratórios (fase pré-clínica), para que só depois de estabelecida a segurança do fármaco e obtidas evidências de que o mesmo é eficaz, sejam iniciados os estudos em humanos (pesquisa clínica), inteiramente acompanhada pela Anvisa.
Pesquisa Clínica
Antes de ser iniciada, a pesquisa clínica deve passar por aprovação de instâncias éticas e também técnicas, para que se tenha a garantia de que os estudos serão conduzidos de maneira correta e segura, garantindo que os voluntários envolvidos obtenham o máximo de benefício e o mínimo de riscos e danos.
Desta forma, o caminho legal para o fornecimento de um medicamento no país é a solicitação do registro, junto à Anvisa, para validação dos dados de qualidade, eficácia e segurança, com as respectivas responsabilidades da empresa, além do monitoramento pós-comercialização (Farmacovigilância) e os estudos clínicos fase IV – que são pesquisas realizadas depois que o produto é comercializado.
ANVISA
Por fim, cabe pontuar que Anvisa é uma autoridade de referência, atua de forma convergente com as melhores agências internacionais, fortalecendo os padrões regulatórios, para que todos os medicamentos tenham qualidade, segurança e eficácia garantida, contribuindo para o uso terapeuticamente correto e custo-efetivo dos medicamentos pelos profissionais de saúde e usuários.
Para saber mais sobre como funciona o processo de registro de medicamentos na ANVISA e em outras agências regulatórias mundias leia o artigo:
Agências regulatórias mundiais e registro de medicamentos
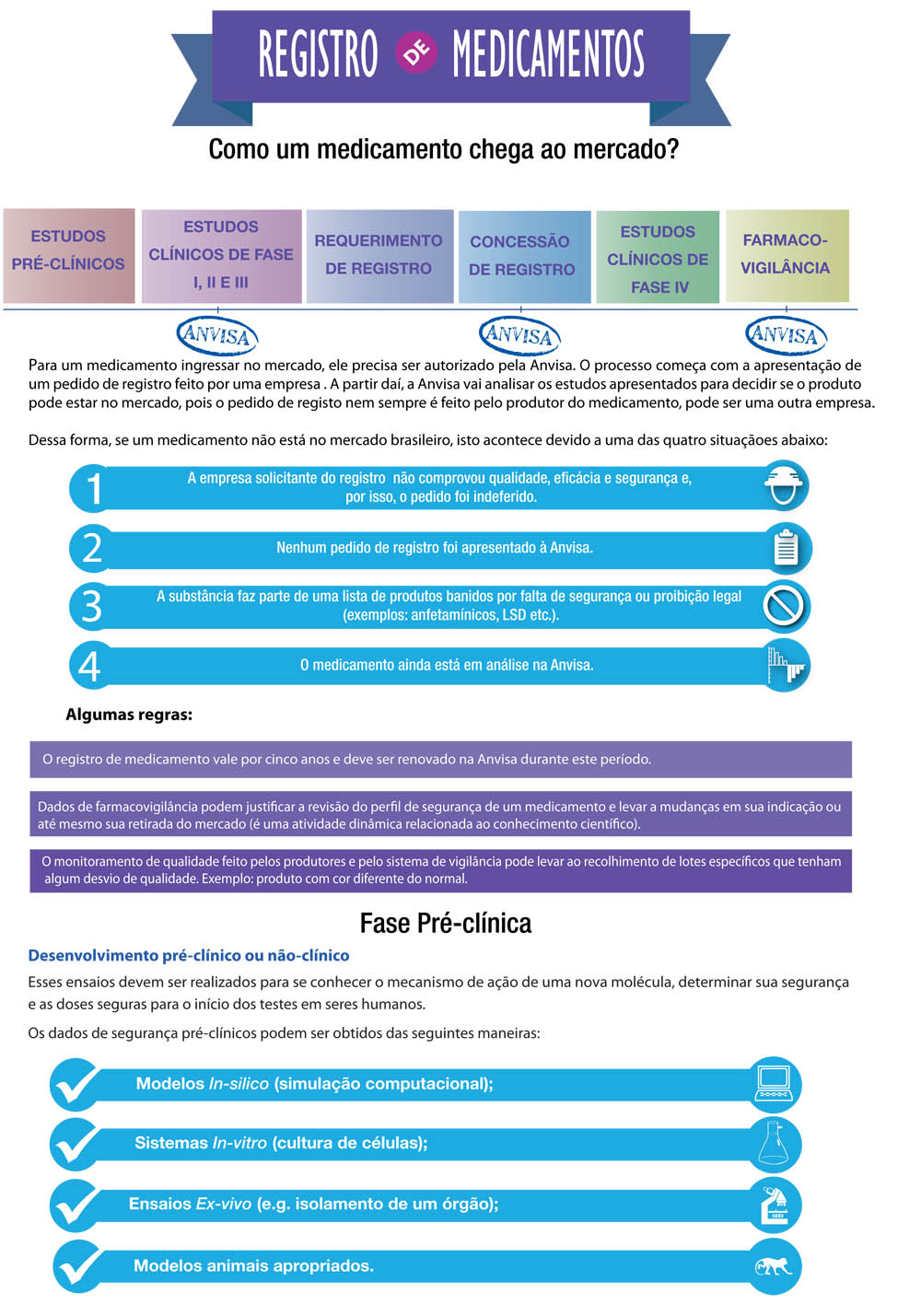
INFOGRÁFICO – REGISTRO DE MEDICAMENTOS – ANVISA
Para entender melhor o processo de registro de medicamentos e o estudo de pesquisa clínica, a ANVISA publicou o infográfico com o passo-a-passo que um novo medicamento deve percorrer para ter seu registro concedido pela Agência e sua consequente disponibilidade no mercado:
Referências
Lei nº. 5.991/1973
ANVISA