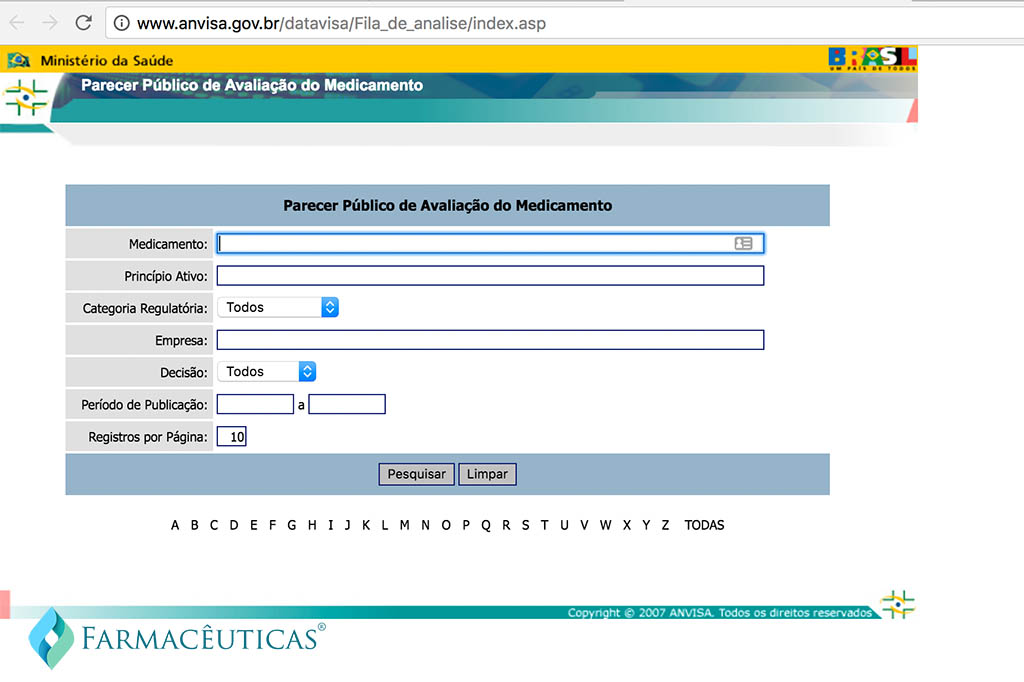
A Anvisa divulgou esta semana o documento chamado de Parecer Público de Avaliação do Medicamento (PPAM) que traz uma síntese da avaliação técnica, incluindo o motivo que levou à aprovação ou reprovação do registro de novos medicamentos. Por meio do Parecer da Anvisa é possível realizar a consulta do processo de registro de novos medicamentos feito pela Agência.
A consulta dos pareceres permite a pesquisa através das seguintes informações:
- Nome do medicamento
- Princípio ativo
- Categoria do medicamento
- Tipo de decisão
- Empresa
- Data
Nos resultados, além do parecer de avaliação, os interessados também poderão encontrar a bula do medicamento e informações como apresentações registradas, local de fabricação, restrição de uso, entre outras informações.
Consulte agora o sistema de Parecer Público de Avaliação do Medicamento
Medicamentos com pareceres públicos disponíveis:
- Produtos biológicos
- Medicamentos novos – aqueles com princípios ativos inéditos no país
- Genéricos inéditos – o primeiro genérico de um determinado medicamento registrado (não inclui genéricos Clone)
- Fitoterápicos, específicos e dinamizados – apenas nos casos de princípio ativo ou associação de princípios ativos inéditos ou de uma nova indicação terapêutica
A lista acima segue a definição adotada pela Anvisa no mês de agosto de 2016 sobre quais pareceres serão divulgados, mas o sistema já contempla medicamentos registrados desde 2014.
Apenas os genéricos inéditos registrados como clones não terão pareceres publicados, pois o medicamento clone é aquele já disponível no mercado rotulado de forma diferente. O que é um medicamento clone?
Quais informações estão no parecer de medicamentos (PPAM)
Os pareceres disponíveis são baseados nas informações apresentadas durante a fase de registro de novos medicamentos na Anvisa e não incluem informações de caráter sigiloso sobre os processos produtivos dos medicamentos.
Os pareceres disponíveis não sofrem atualizações após o registro. Porém, as informações relativas à apresentação, embalagem, local de fabricação, prazo de validade e cuidados de conservação que aparecem ao clicar no nome do medicamento serão sempre atualizadas para o produto.
Até agosto de 2016, os pareceres estavam disponíveis com o nome de [quote_center]Bases técnicas e científicas para aprovação/reprovação do registro de medicamentos.[/quote_center]
Os pareceres também podem ser consultados na página de Registros e Autorizações no site da ANVISA.
Regularização de Produtos – Medicamentos – ANVISA
Informações Gerais disponibilizadas pela ANVISA
O procedimento simplificado – clone visa reduzir significativamente o tempo para concessão de registro, considerando as recorrentes solicitações de registro de um mesmo medicamento por diferentes empresas e, ainda, as solicitações do mesmo medicamento, por exemplo, como similar e genérico, pela mesma empresa.
O procedimento simplificado – clone visa reduzir significativamente o tempo para concessão de registro, considerando as recorrentes solicitações de registro de um mesmo medicamento por diferentes empresas e, ainda, as solicitações do mesmo medicamento, por exemplo, como similar e genérico, pela mesma empresa.
Processo matriz é o processo no qual constam todas as informações necessárias à solicitação de registro de um medicamento – relatório técnico e clínico – e que será vinculado a um ou mais processos clones. Para que o processo seja eleito como matriz de um processo clone, ele deve que estar adequado, segundo os critérios estabelecidos na RDC nº 31/2014.
Em relação à condição da empresa, para o deferimento de registro do processo clone, será observada apenas a condição de satisfatoriedade da empresa peticionante (clone) junto à atual Gerência-Geral de Inspeção e Fiscalização Sanitária (GGFIS), para assegurar que a empresa possui um sistema de garantia da qualidade eficiente.
Assim como todas as outras etapas do processo de fabricação, o controle de qualidade do medicamento registrado pelo procedimento simplificado – clone tem que ser feito assim como é feito para o medicamento do processo matriz. A empresa clone é responsável pela avaliação e liberação dos lotes do medicamento registrado por ela.