Não é de hoje que o mercado internacional vem alertando sobre a presença de aminas (nitrosaminas – impurezas genotóxicas) acima dos limites considerados como tóxicos para humanos em lotes de medicamentos da família das losartanas e valsartanas.
Nos últimos oitos meses, o FDA, entre outras agências reguladoras internacionais, tem recebido recalls (recolhimento) de medicamentos e insumos farmacêuticos ativos (IFAs) contaminados com nitrosaminas.
A questão é que as sustâncias ativas losartana e valsartana não possuem alta toxicidade, dentro da dosagem recomendada para o tratamento, e são rotineiramente utilizadas nos casos de hipertensão arterial, no entanto, estas substâncias possuem como produto de degradação nitrosaminas com alto potencial genotóxico (impurezas genotóxicas), ou seja, com grande potencial de carcinogenicidade (potencial cancerígeno), mutagenicidade (potencial ação de mutação) e teratogenicidade (potencial ação de deformidade fetal – mulheres grávidas). Desta forma, as nitrosaminas são prováveis carcinógenos humanos.
Impurezas genotóxicas nos medicamentos para hipertensão arterial
Os produtos estão associados à produção de bloqueadores dos receptores da angiotensina II (ARBs), principalmente a valsartana, entre outros medicamentos de sua família (ex: losartana).
As duas impurezas de nitrosaminas que são geralmente encontradas são N-Nitrosodimetilamina (NDMA) e N-Nitrosodietilamina (NDEA).
Essas duas substâncias são amplamente encontradas em água e alimentos, mas a FDA declarou que sua “presença em produtos farmacêuticos é inaceitável”.
A quantidade de ingestão diária segura para as nitrosaminas suspeitas é de 0,096 μg / dia. No entanto, a quantidade geralmente encontrada nos comprimidos varia de 0,3 μg / comprimido a 20 μg / comprimido, claramente acima do limite seguro estabelecido pelo FDA.
O FDA ainda tem sido claro em apontar que nem todos os lotes de produtos dessa família de medicamentos têm níveis inaceitáveis.
E para controlar a quantidade de tais impurezas genotóxicas o FDA publicou métodos analíticos adequados para medir NDMA e NDEA em medicamentos das famílias da valsartana.
A Comunidade Europeia também tem recebido muitos casos de recall, e está atuando de forma intensa para determinar as causas principais das impurezas, além de estabelecer medidas preventivas para a recorrência destes problemas.
O FDA relata seu esforço como um “esforço exaustivo” para determinar as causas.
Entre as possíveis causas que estão sendo investigadas são:
- Subprodutos do processo de síntese
- Reutilização de solventes
- E possivelmente as duas situações somadas
As Nitrosaminas (impurezas genotóxicas) são geralmente formadas pela reação de nitrito de sódio com as aminas secundárias. Embora nenhum deles seja necessário na síntese da valsartana, em uma rota sintética, o nitrito de sódio é usado para destruir o excesso de azida sódica usada na síntese da IFA.
Se a DMF (dimetilformamida), que é o solvente usado na síntese da IFA, continha dimetilamina residual, isto poderia levar à formação de NDMA.
As impurezas genotóxicas dos medicamentos de pressão alta e a ANVISA
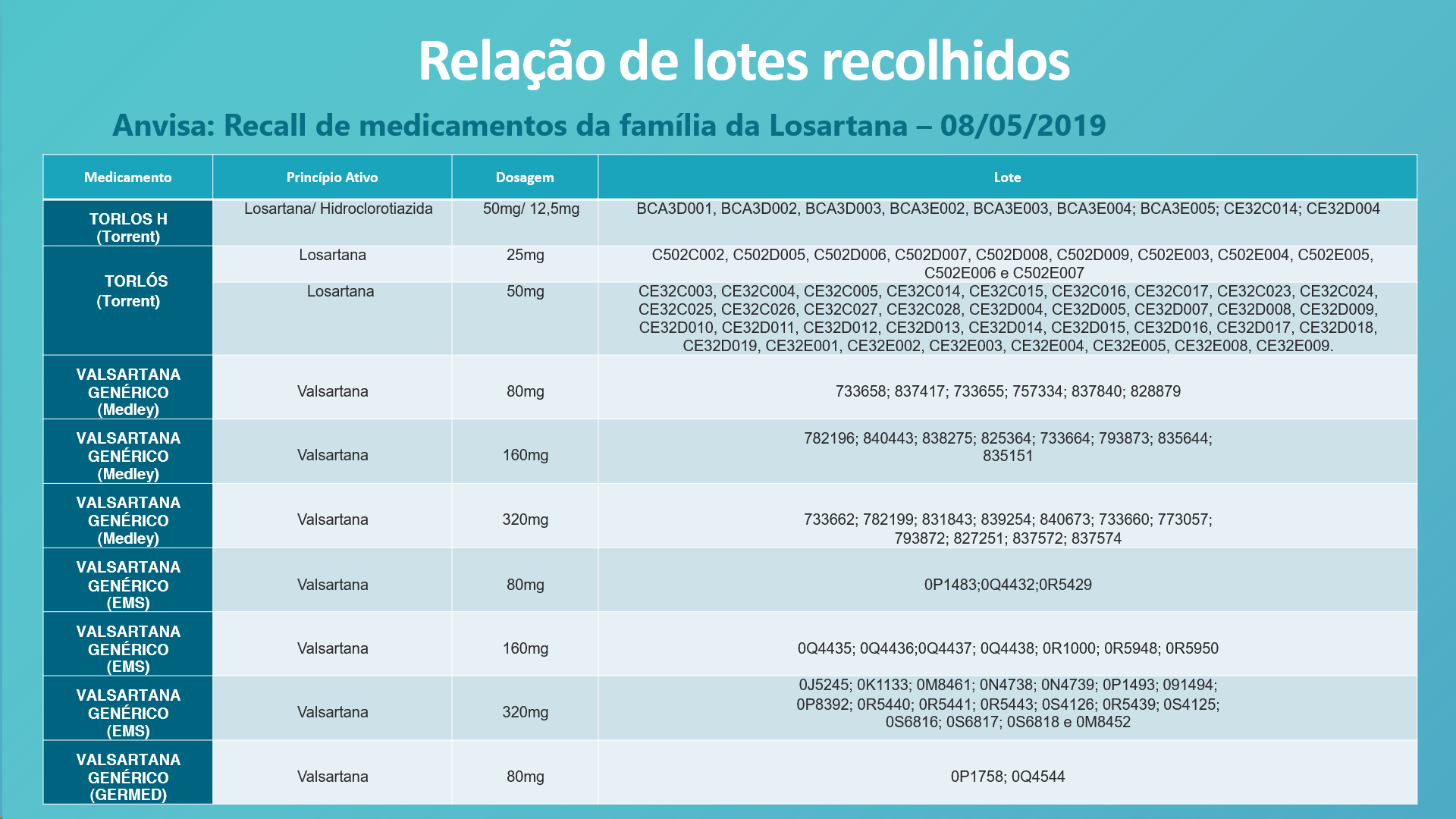
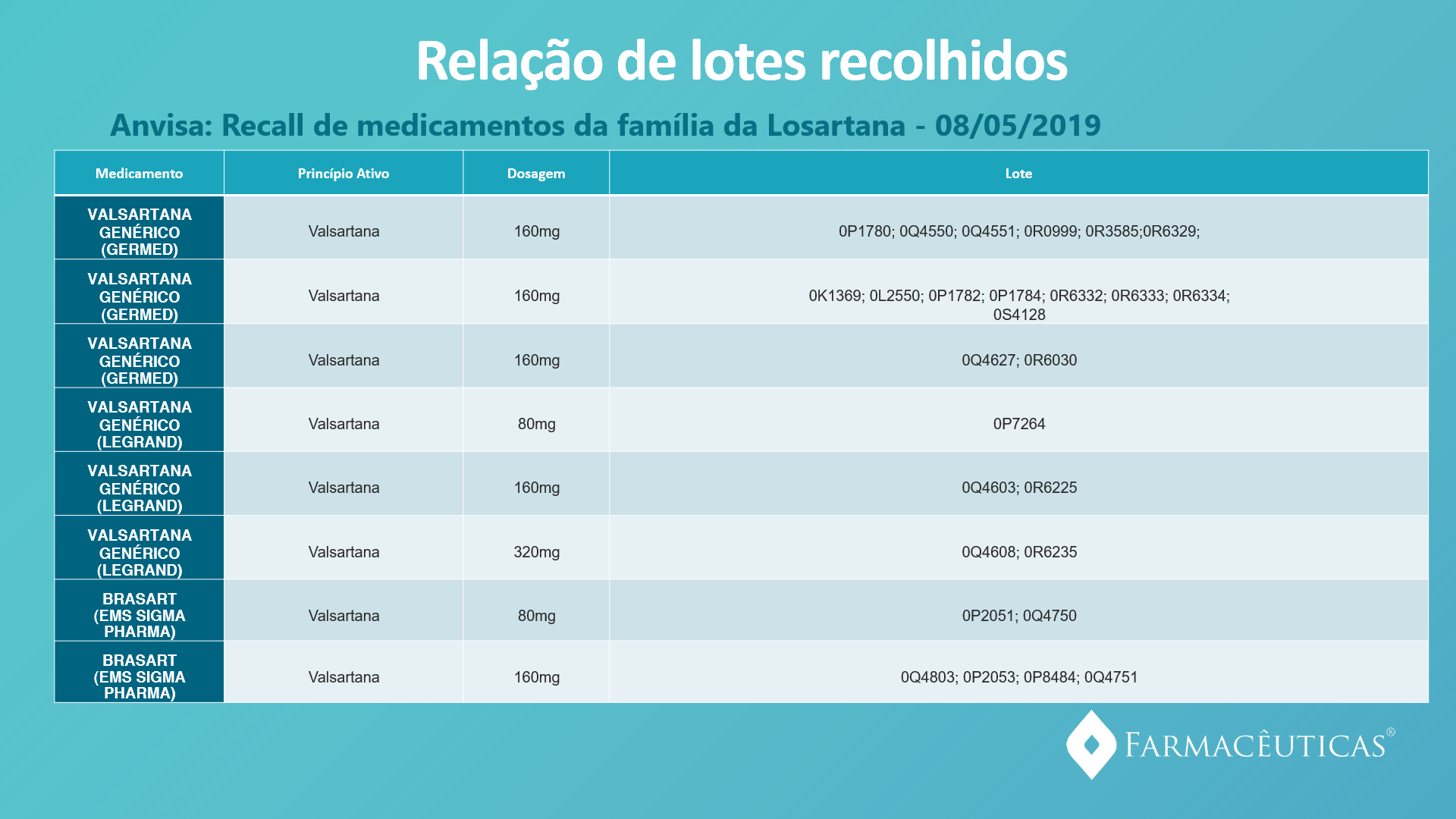
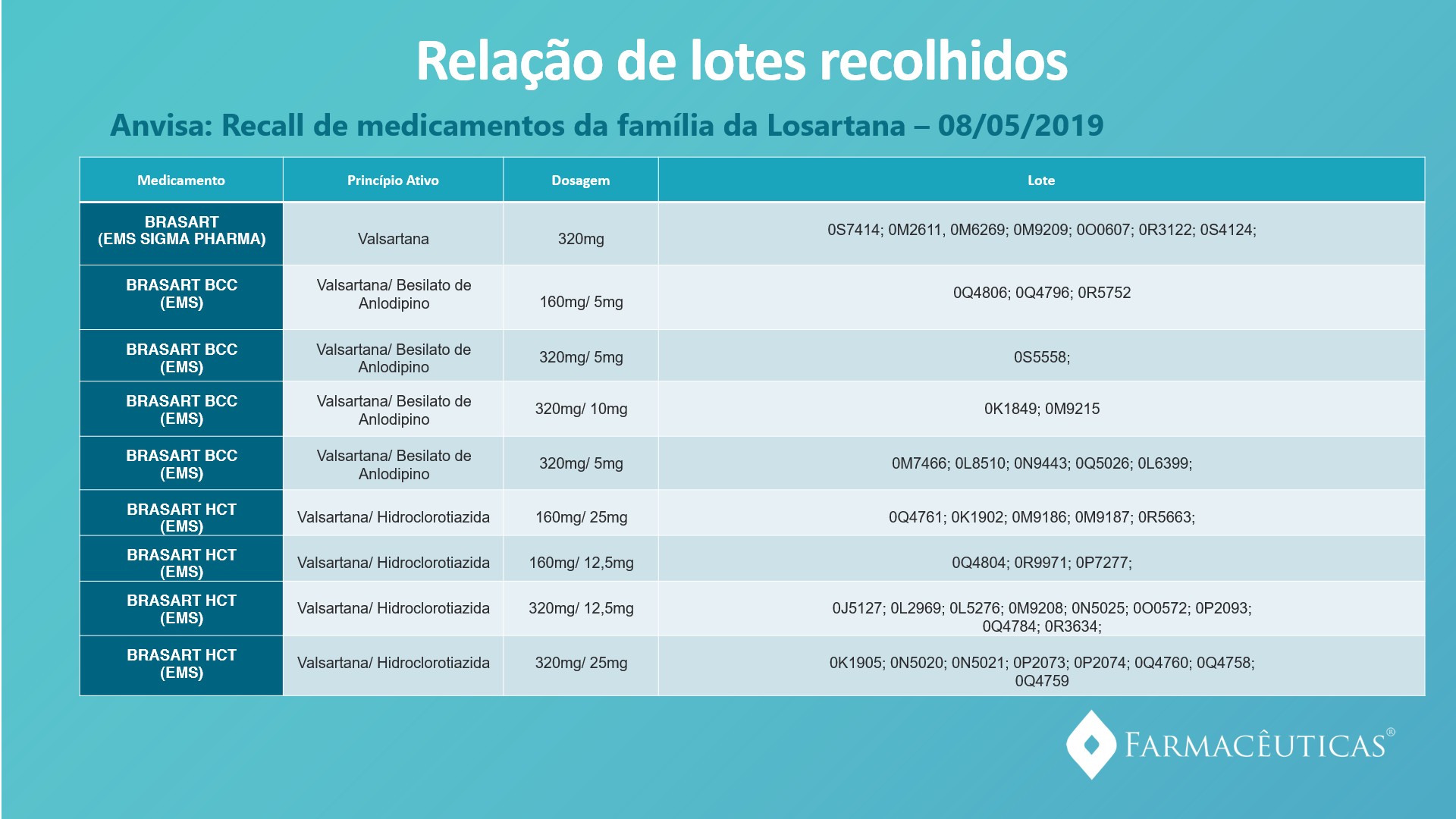
Foi publicado no site da ANVISA (08/05/2019) uma ação de recolhimento de medicamentos da família das losartanas de diversos lotes de fabricantes dos medicamentos.
A Anvisa já vinha há algum tempo verificando este assunto a ponto de tomar esta medida para o bem da saúde da população.
E agora uma das medidas já executadas pelo órgão é a determinação do recolhimento de lotes específicos do produto.
Para explicar o assunto, a Anvisa publicou uma nota com várias informações sobre o tema para esclarecer e orientar a população:
Medidas da Anvisa
O recolhimento determinado pela Agência atinge apenas lotes específicos de medicamentos, estratégia adotada em diversos países para os mesmos produtos. Desde julho de 2018, a Anvisa tem realizado publicações e ações alinhadas com agências do mundo inteiro, tais como a Agência de Medicamentos e Alimentos dos Estados Unidos da América (FDA) e a Agência Europeia de Medicamentos (EMA), visando a segurança da saúde da população e a qualidade dos produtos consumidos.
No Brasil, além do recolhimento de lotes de medicamentos, as ações da Anvisa incluem a suspensão da fabricação, importação, distribuição, comercialização e uso dos insumos farmacêuticos ativos com suspeita de contaminação. No total, foram efetuadas 14 suspensões de três insumos (losartana, valsartana e irbesartana) de dez fabricantes internacionais.
Também foi determinada a fiscalização de todas as empresas fabricantes de medicamentos contendo “sartanas” disponíveis no mercado brasileiro. Até o momento, foram avaliadas 29 empresas e 111 medicamentos comercializados em 2018. Com relação ao recolhimento, ao todo os lotes recolhidos já somam aproximadamente 200.
A Anvisa também determinou a avaliação dos processos de qualificação dos fornecedores para os medicamentos à base de “sartanas” e a realização de testes para os produtos com insumos farmacêuticos ativos com possível formação de nitrosaminas durante a sua síntese química, entre outras medidas.
“É importante notar que essa é uma ação conjunta, que envolve esforços da Anvisa e de todos os fabricantes dos medicamentos, que estão ajudando a detectar quais são os lotes afetados pelo problema e voluntariamente recolhendo os produtos do mercado”, informa o gerente geral da área de Inspeção e Fiscalização Sanitária (GGFIS) da Agência, Ronaldo Gomes.
Para o consumidor, a Anvisa preparou uma lista com os números de lotes dos medicamentos que devem ser recolhidos, que pode ser rapidamente consultada. Basta verificar o número do lote que consta na caixa do medicamento e conferir aqui.
Baixo risco
Embora o risco seja muito pequeno, estudos apontam que as nitrosaminas têm potencial ou provável risco de causar câncer caso os medicamentos sejam consumidos todos os dias, em sua dose máxima, durante cinco anos seguidos.
Nessas condições, autoridades europeias calcularam que o risco de câncer associado ao consumo contínuo do medicamento é de 0,00017%, ou um caso para cada grupo de 6.000 pessoas. Portanto, o risco é muito baixo e está associado ao consumo diário e contínuo, em altas doses e por um longo período.
Por estes motivos, a Anvisa esclarece que o consumo desses medicamentos não oferece risco imediato para as pessoas que fazem uso deles e que eles são eficazes para o tratamento de pressão alta, mas recomenda que sejam trocados por outro de igual valor terapêutico.
Manutenção do tratamento
Para quem tem em casa o medicamento com o mesmo número de algum lote recolhido, a Agência orienta que o tratamento de hipertensão não seja interrompido até que se faça a troca por outro medicamento. Isso porque a interrupção pode causar sérios prejuízos imediatos, como risco de morte por derrame, ataques cardíacos e insuficiência renal.
De acordo com a Anvisa, existem diversas alternativas medicamentosas para terapias de pressão alta e, por isso, não há risco de desabastecimento ou falta de medicamentos. Ou seja, há no mercado brasileiro medicamentos da mesma classe terapêutica e com os mesmos princípios ativos e concentração.
A troca do medicamento deve ser feita mediante orientação de um médico ou de um farmacêutico. O cidadão também pode entrar em contato com a empresa, por meio do serviço de atendimento ao consumidor, e solicitar a troca do seu medicamento que consta na lista de lote recolhido.
A importância do Estudo de Holding Time para as indústrias farmacêuticas.
O estudo de Holding Time sempre foi importante justamente para avaliação o comportamento das matérias-primas e dos produtos submetidos às condições de armazenamento durante a fase produtiva, muitas vezes sem padronização e controle.
É justamente com este tipo de validação que conseguimos comprovar o comportamento em termos de suscetibilidade ao crescimento microbiano, polimorfismo, aparecimento de compostos de degradação, entre outros aspectos, que impactam diretamente na qualidade do produto acabado (medicamento).
Sendo assim, fica aqui a lição de casa para as empresas fabricantes de medicamentos para que novos recolhimentos não aconteçam.
E se quiserem mais informações participem de nossos cursos de Holding Time. Próxima turma na semana que vem:
https://cursosfarmaceuticas.com.br/produto/curso-de-holding-time-presencial-sao-paulo/
Referências
- FDA
- Toxnet – https://toxnet.nlm.nih.gov/
- Anvisa
- Destin Le Blanc – Cleaning Memo for March 2019 – Contaminants in API Manufacture