A ANVISA aprovou nesta segunda feira, dia 09/10/2017, por meio do Diário Oficial da União – DOU – o Produto biológico Tecentriq (atezolizumabe) indicado para o tratamento de câncer de bexiga e pulmão (carcinoma urotelial e câncer de pulmão de não-pequenas células).
Sobre o novo tratamento de câncer de bexiga e pulmão
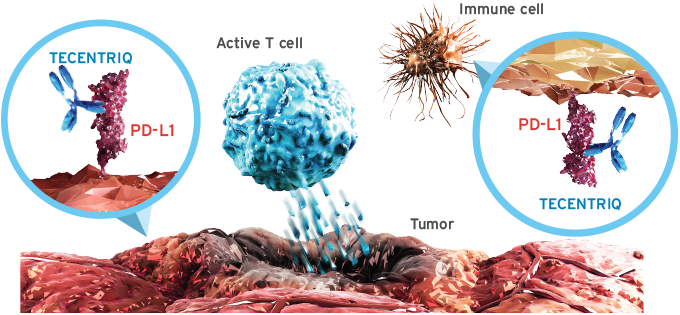
A substância ativa do Tecentriq, o atezolizumabe, é um anticorpo monoclonal, sendo um tipo de proteína projetada para reconhecer e se conectar à proteína PD-L1, que está presente na superfície de muitas células cancerosas. É indicado para o tratamento de câncer de bexiga e pulmão (carcinoma urotelial e câncer de pulmão de não-pequenas células).
O PD-L1 atua para “desligar” células imunes que, de outra forma, atacariam as células cancerígenas. Ao se conectar ao PD-L1 e reduzir seus efeitos, o atezolizumabe aumenta a capacidade do sistema imunológico para atacar as células cancerosas e, assim, diminuir a progressão da doença.
O produto Tecentriq (atezolizumabe) foi aprovado para as seguintes indicações terapêuticas:
- Como monoterapia, é indicado para o tratamento de pacientes adultos com carcinoma urotelial (UC) localmente avançado ou metastático após quimioterapia prévia à base de platina ou que sejam considerados inelegíveis à cisplatina.
- Como monoterapia, é indicado para o tratamento de pacientes adultos com câncer de pulmão de não-pequenas células (CPNPC) localmente avançado ou metastático após quimioterapia prévia. Pacientes com mutações ativadoras EGFR ou mutações tumorais ALK positivo devem ter recebido terapia alvo para essas alterações antes de serem tratados com Tecentriq.
Fonte
ANVISA – 09/10/2017 15:42